研究内容
私たちは、タンパク質の「バイオジェネシス」を研究します
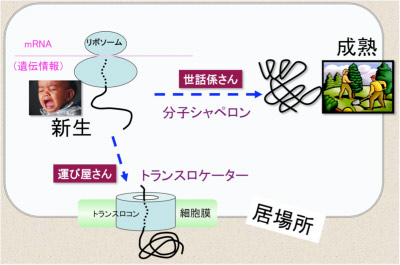
生命現象は「ゲノムから細胞へ」という基本的見方で捉えることができます。このスキームの中核となるのは「遺伝子の子供たち」である個性的なタンパク質たちの振る舞いです。彼らは遺伝子によって決まる順番でアミノ酸が数珠つなぎになったポリペプチド鎖として誕生します。細胞にはそのような新生ポリペプチド鎖のケアをする様々な装置が存在しており、タンパク質たちの形づくり(フォールディング、立体構造形成)、それぞれの居場所への移動と配置(トランスロケーション、局在化)、他のタンパク質や細胞成分との会合(アセンブリー、複合体形成)などが的確に起こるよう働いています。一方で、タンパク質たちは、不必要・邪魔になるものは分解されて行くという分解(品質管理)も受けています。このようにして、生命活動の主役を担うタンパク質たちが生き生きと活躍する細胞というミクロ社会が出来上がっていきます。私たちは、タンパク質たちの誕生から成熟、そして死に至る過程がどのように制御されているかについて研究しています。
具体的には、どんなことを取りあげているの?
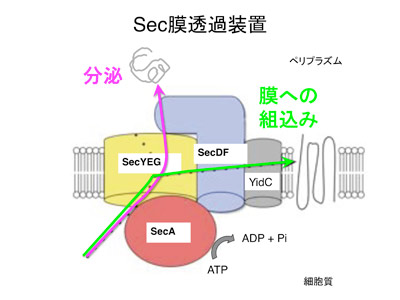
私たちは、新生タンパク質の膜を越えた動きを可能とする、ポリペプチド膜透過チャネル(トランスロコン)の中心となる膜タンパク質SecY(高等生物ではSec61と呼ばれる)を大腸菌を用いて発見し、一連の研究を行って来ました。分泌タンパク質は、翻訳された後、折り畳まれることなく膜に受け渡されます。そして、SecY複合体とモータータンパク質 SecAなどの協同作用によって、「イオンをも通さない膜を越える」と言う一大イベントを成し遂げます。膜タンパク質が膜に組み込まれることも細胞にとって重要ですが、ここでもSecYトランスロコンが活躍し、膜タンパク質YidCの関与も知られています。これらの研究については、これまでの発表論文を見ていただくことして、現在主に取り組んでいることを説明します。私たちは、上で登場したSecAやYidCが、翻訳途上のポリペプチドが主役となる全く新しい仕組みによる発現制御を受けていることを見いだしました。
「生まれかけ」で働く制御ポリペプチド
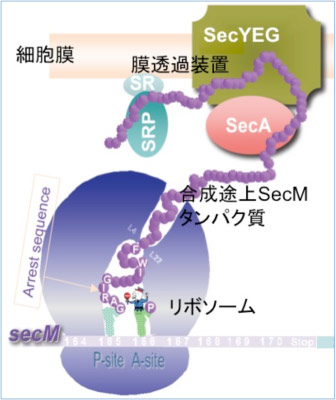
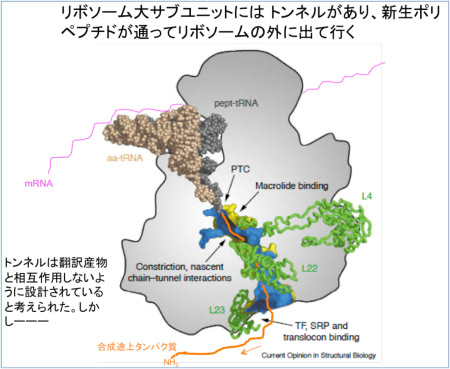
タンパク質は通常リボソームの外に生まれ落ちてから働くものと考えられていますが、私たちは生まれかけの状態で、リボソームの内部で翻訳にブレーキをかける能力を持つタンパク質を発見し、それらがSecA, YidCと言ったタンパク質輸送因子の発現を制御していることを明らかにしました。大腸菌の分泌モニタータンパク質SecMはsecA遺伝子の上流域(一続きのmRNAとして転写される)からコードされる分泌タンパク質です。そのC末端付近のアミノ酸配列は、リボソーム内部の新生ポリペプチド鎖脱出トンネルと相互作用する性質があり、その結果自らの翻訳伸長を停止させます(翻訳アレスト)。リボソームがmRNA上で立ち往生すると、mRNAの二次構造が破壊されてsecAの翻訳が可能になります。一方、SecMのN末端領域がリボソームの外でSecA-SecY膜透過装置に認識されて膜透過を起こすと、翻訳アレストが解除され、SecAの翻訳は低下します。膜透過が遅延すれば翻訳アレストが長引き、SecAの翻訳が上昇します。このようにSecMは、合成途上で自らの分泌状態に呼応した翻訳アレストによって、SecAの発現を制御します。枯草菌の膜挿入モニタータンパク質MifMはSecMとは異なる翻訳アレスト配列を持ち、SecMと同様の機構で、YidC2の翻訳を自らの膜挿入状態を感知して制御することも明らかになりました。
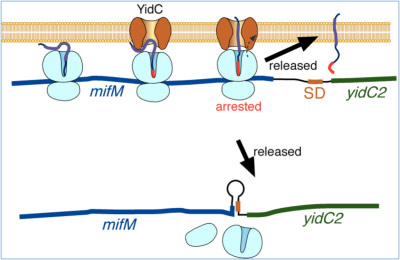
合成途上鎖(nascent chain)の分子生物学
私たちの研究により、アミノ酸配列の中にはリボソームが翻訳を苦手とするものがあることがわかりました。すなわち、リボソームはどのような配列でも一様な速度で翻訳するわけではありません。そして、「翻訳のスピードが合成途上鎖自体の動的状態により影響される」というフィードバック機構の存在も明らかになりました。私たちは、より一般的に、一次配列に基づく翻訳スピードの微調整により、翻訳途上ポリペチプド鎖の挙動が制御され、出来上がるべきタンパク質の運命−−例えば、行き先の決定、立体構造の獲得、パートナーの獲得−−が影響されるのではないかと考えています。そして、細胞に於ける合成途上鎖(まだtRNA分子が結合しているポリペプチド鎖)の全体像("nascentome"と命名)を可視化する新たな実験方法を開発するなどして、この問題にチャレンジしています。
私たちの実験系: モデル生物を使った分子謎解き

大腸菌は分子生物学の起源となり、遺伝子の働きの基本が解明された生物です。枯草菌は胞子形成という「細胞分化」を行う原核生物として特徴的で、細胞分裂などの研究が進んでいます。これらは、分子レベル、細胞レベルでの様々な知識が最も詳しく蓄積した「モデル生物」です。私たちは、このような材料を使うことにより、緻密な謎解きができること、そしてまだまだ新たな「概念」の発掘が可能であることに魅力を見いだしています。高等生物の理解にも役立つ「パラダイムシフト」を目指して地道に研究を進めます。学生(院生)の時に基礎研究の経験を積むことは、将来どのような道に進むにしても、力となるものと考えています。学生諸君の参加を歓迎します。
|
